Syniadau i wella gwaith ymarferol electrolysis
David Everett suggests ideas for enhancing electrolysis practical work
This article is also available in English
Read the English language version.

Pam astudio electrolysis?
Mae electrolysis wrth galon cynhyrchu alwminiwm, puro copr, a chynhyrchu sodiwm hydrocsid a chlorin. Bydd y myfyrwyr yn gwerthfawrogi pa mor berthnasol yw’r prosesau hyn ar ôl darganfod bod faint o’r cemegion hyn sy’n cael eu cynhyrchu yn y byd bob blwyddyn yn cael ei fesur mewn megatunelli (tabl 1, isod).
Bydd y prosesau electrolytig y bydd y myfyrwyr yn eu gweld yn y labordy yn cael eu rhoi mewn persbectif diwydiannol drwy wylio clipiau fideo fel rhai’r adnodd ar-lein Alchemy?.
Bydd y prosesau electrolytig y bydd y myfyrwyr yn eu gweld yn y labordy yn cael eu rhoi mewn persbectif diwydiannol drwy wylio clipiau fideo fel rhai’r adnodd ar-lein Alchemy?.4
Mae electrolysis a’i gymwysiadau yn ymddangos ym mhob manyleb arholiad TGAU. Mae gwaith ymarferol sy’n seiliedig ar electrolysis yn weithgaredd gofynnol wrth asesu sgiliau ymarferol myfyrwyr (tabl 2, isod).
Cemeg greiddiol a chynnydd
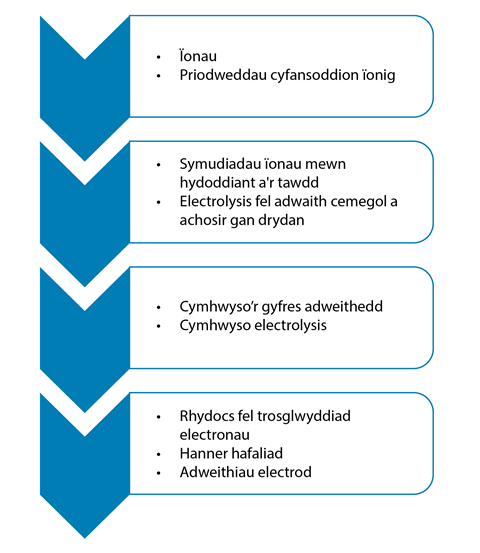
Nid yw electrolysis yn ymddangos ar ei ben ei hun mewn cynlluniau gwaith ac mae’n bwysig ystyried yr wybodaeth flaenorol sydd ei hangen ar fyfyrwyr i’w ddeall.
Yn gynharach, bydd myfyrwyr yn dysgu am ïonau a phriodweddau sylweddau ïonig. Byddan nhw’n dysgu bod ïonau yn gallu symud pan fyddan nhw mewn hydoddiant neu yn y tawdd, ac y bydd yr electrolyt hwn yn dargludo cerrynt trydanol. Mae’n gam bach iddyn nhw wedyn werthfawrogi bod electrolysis yn adweithiau cemegol sy’n cael eu hachosi gan lif cerrynt.
Wrth i’r myfyrwyr ymchwilio i wahanol brosesau electrolysis, gallan nhw gymhwyso eu gwybodaeth am y gyfres adweithedd i egluro’r cynhyrchion sy’n cael eu ffurfio, yn enwedig pan fydd sawl posibilrwydd. Bydd gwybodaeth am y gyfres adweithedd yn eu helpu i ddeall pam mae hydrogen yn cael ei gynhyrchu wrth yr electrod negatif pan fydd sodiwm clorid dyfrllyd yn cael ei electroleiddio, ond bod copr yn cael ei gynhyrchu wrth yr electrod hwn pan ddefnyddir copr(II) clorid dyfrllyd.
Ar lefel uwch, bydd myfyrwyr mwy galluog yn dod i ddeall bod electronau’n cael eu trosglwyddo wrth yr electrodau. Mae hanner hafaliadau’n cael eu defnyddio i ddisgrifio adweithiau’r electrodau ac mae hyn yn cysylltu ag astudiaethau ôl-16, pan fydd potensial rhydocs yn cael ei ddefnyddio i esbonio ac i gyfiawnhau’r gyfres adweithedd.
Datblygu sgiliau ymarferol
Mae’n bwysig bod gwaith ymarferol myfyrwyr yn ddiddorol, yn rhoi canlyniadau clir sy’n galluogi dehongliad cadarnhaol o’r arsylwi, yn gweithio’n ddibynadwy ac y gellir ei wneud yn ddiogel.
Mae’r rhan fwyaf o fyrddau arholi’r DU yn rhoi hyblygrwydd i athrawon o ran sut cynhelir arbrofion electrolysis ac o ran y dewis o hydoddion yr ymchwilir iddynt. Mae’n ddymunol bod myfyrwyr yn ymgymryd â’r arbrofion hyn mewn ffordd ymchwiliol yn hytrach na dilyn rysáit gyda chanlyniadau disgwyliedig. Mae cynnal cyfres o arbrofion ar nifer o hydoddion a phrofi’r cynhyrchion yn caniatáu i’r myfyrwyr ddadansoddi eu harsylwadau ac ymchwilio i beth yw’r cynhyrchion. Gall y myfyrwyr wedyn ddarganfod sut mae’r cynhyrchion yn berthnasol i waith maen nhw wedi’i wneud ar y gyfres adweithedd. Bydd hyn yn cysylltu â gwaith mewn cyrsiau ôl-16 ar botensial rhydocs.
Bydd angen i’r myfyrwyr ymarfer drwy ddefnyddio celloedd electrolytig er mwyn bodloni gofynion byrddau arholi a dangos eu bod wedi ennill y sgiliau angenrheidiol. Bydd defnyddio rhai mathau o gyfarpar yn atal athrawon rhag trefnu digon o waith ymarferol oherwydd y gost, faint o gemegion a ddefnyddir, y peryglon posibl sy’n gysylltiedig â’r broses a’r angen am ddigon o bŵer. Serch hynny, mae yna ddewisiadau eraill ar gael.
Dull synoptig
Enghraifft: electrolysis hydoddiannau halwynau dyfrllyd
Dyma rai cwestiynau posibl er mwyn i’ch myfyrwyr gael dechrau arni:
- Pa halwynau fyddwch chi’n ymchwilio iddyn nhw?
- Ble yn y gyfres adweithedd mae’r metelau sydd yn yr halwynau hyn?
- Pa gyfarpar byddwch chi ei angen?
- Sut gallwch chi gasglu unrhyw nwyon sy’n cael eu cynhyrchu wrth yr electrodau?
- Sut ydych chi wedi profi nwyon o’r blaen i’w hadnabod?
Cynllunio’r gweithgaredd
Eglurwch sut byddech chi’n gwneud pob cam yn eich ymchwiliad. Rhowch fanylion yr holl gyfarpar a chemegion sydd eu hangen a’r gweithdrefnau i’w defnyddio.
Problemau ymarferol a datrysiadau posibl
Gwella’r canlyniadau
Gydag electrolysis halwynau copr(II) ar raddfa fawr, mae hi’n anodd gweld y dyddodiad copr ar yr electrod negatif drwy’r hydoddiant glas tywyll, a phrin mae modd gweld y gostyngiad yng nghrynodiad yr ïonau copr(II). Ar ben hynny, gydag electrolysis hydoddiannau cloridau, mae datblygiad llawer iawn o glorid yn gallu achosi gofid i fyfyrwyr ac i athrawon.
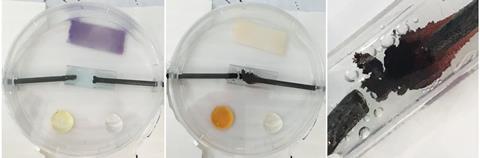
Serch hynny, mae modd cynnal fersiwn ar raddfa micro o electrolysis o gopr (II) clorid dyfrllyd gyda dim ond dau neu dri diferyn o’r hydoddiant (ffigur 2). Mewn ychydig funudau, mae’r lliw glas yn pylu i fod bron yn ddi-liw, mae’r clorin sy’n cael ei gynhyrchu wrth yr electrod positif yn troi papur litmws glas yn goch ac yna’n cael ei gannu, ac mae diferyn o botasiwm ïodid dyfrllyd yn troi’n frown. Mae’r myfyrwyr yn gallu gweld y newidiadau hyn yn hawdd a chasglu beth yw’r cynhyrchion sydd wrth yr electrodau. Mae’r swm bach iawn o glorin sy’n cael ei gynhyrchu yn cael ei amsugno i raddau helaeth gan adweithyddion y prawf ac mae unrhyw beth sydd dros ben yn cael ei gyfyngu o dan gaead y ddysgl Petri.
Mae modd defnyddio blychau plastig tec-awê i storio ac i ddosbarthu’r holl gyfarpar a chemegion ar gyfer arbrawf ar raddfa micro. Mae’r rhain yn ei gwneud hi’n haws trefnu gwers ymarferol ac yn golygu nad oes angen i’r myfyrwyr fynd o amgylch y labordy i gasglu’r cyfarpar.
Anodau a chatodau
Yn yr erthygl hon rwyf wedi osgoi defnyddio’r termau anodau a chatodau oherwydd eu bod yn gallu drysu myfyrwyr: yr anod yw’r electrod positif mewn electrolysis ond yr electrod negatif mewn celloedd electrocemegol. Wrth ddefnyddio’r term anod gyda’ch myfyrwyr, mae’n bwysig pwysleisio mai dyma’r electrod lle mae ocsideiddio’n digwydd.
Yn yr erthygl hon rwyf wedi osgoi defnyddio’r termau anodau a chatodau oherwydd eu bod yn gallu drysu myfyrwyr: yr anod yw’r electrod positif mewn electrolysis ond yr electrod negatif mewn celloedd electrocemegol. Wrth ddefnyddio’r term anod gyda’ch myfyrwyr, mae’n bwysig pwysleisio mai dyma’r electrod lle mae ocsideiddio’n digwydd.7
Cyfarpar electrolysis

Ar lefel TGAU, dim ond electrolysis o hydoddiannau halwynau dyfrllyd y mae’n rhaid i fyfyrwyr ei wneud. Serch hynny, bydd hefyd angen iddyn nhw wybod am electrolysis halwynau tawdd. Yn hytrach na dangos clipiau fideo, efallai bydd athrawon eisiau dangos y broses hon, ond nid yw’n syml. Mae plwm bromid a sinc clorid yn cael eu defnyddio’n aml, ond os caiff hyn ei wneud ar y raddfa a awgrymir fel rheol, rhaid gwneud yr arddangosiad mewn cwpwrdd gwyntyllu ac mae’r crwsibl anhryloyw yn ei gwneud yn anodd i fyfyrwyr arsylwi ar yr halwyn tawdd. Mae defnyddio dull ar raddfa micro yn goresgyn y naill broblem a’r llall ac mae hi’n hawdd gweld y broses (ffigur 3).
Ar lefel TGAU, dim ond electrolysis o hydoddiannau halwynau dyfrllyd y mae’n rhaid i fyfyrwyr ei wneud. Serch hynny, bydd hefyd angen iddyn nhw wybod am electrolysis halwynau tawdd. Yn hytrach na dangos clipiau fideo, efallai bydd athrawon eisiau dangos y broses hon, ond nid yw’n syml. Mae plwm bromid a sinc clorid yn cael eu defnyddio’n aml, ond os caiff hyn ei wneud ar y raddfa a awgrymir fel rheol,5 rhaid gwneud yr arddangosiad mewn cwpwrdd gwyntyllu ac mae’r crwsibl anhryloyw yn ei gwneud yn anodd i fyfyrwyr arsylwi ar yr halwyn tawdd. Mae defnyddio dull ar raddfa micro yn goresgyn y naill broblem a’r llall ac mae hi’n hawdd gweld y broses (ffigur 3).
Does dim angen defnyddio cyflenwad pŵer DC drud ar gyfer gwaith ymarferol: weithiau bydd myfyrwyr yn camddefnyddio hwn gan chwythu ffiwsiau neu switshis tripio. Yn aml, bydd batri PP3 9V syml gyda chysylltwyr a chlipiau crocodeil yn fwy na digon ac yn osgoi’r problemau hyn.
Mae rhodenni carbon neu ‘blwm’ pensil (graffit) yn aml yn cael eu defnyddio fel electrodau mewn arbrofion ysgol. Yn anffodus, maen nhw’n frau ac yn hawdd eu torri a gall hyn fod yn broblem wrth eu rhoi mewn drwy dopyn: nid yw’n hawdd gweld toriadau ac mae’r myfyrwyr yn gallu meddwl nad yw’r cyfarpar yn gweithio. Dewis arall yw defnyddio rhodenni ffibr-carbon 2 mm fel electrodau. Mae’r rhain yn cael eu gwerthu i adeiladu fframiau barcud, gan eu bod yn ysgafnach, yn galetach ac yn gryfach na rhodenni cansen traddodiadol. Mae modd eu torri’n ddarnau byr (drwy ddefnyddio gefeiliau cryf) a gwneud electrodau rhagorol na fyddan nhw’n torri wrth eu defnyddio.
Mae hi’n gallu bod yn anodd i fyfyrwyr gasglu nwy o electrod drwy ddefnyddio tiwb profi a’i ben i lawr wedi’i lenwi â hydoddiant: yn anochel bydd yr hydoddiant yn tywallt allan o’r tiwb. Dewis arall yw defnyddio chwistrell gyda phen y faril wedi’i dorri i ffwrdd (ffigur 4). Gwthiwch y plymiwr i mewn a gostwng y chwistrell i mewn i’r gell uwchben yr electrod. Tynnwch y plymiwr yn ôl i dynnu electrolyt i mewn i’r chwistrell dros yr electrod – mae nawr yn barod i gasglu nwy. Mae modd defnyddio’r graddnodau ar y chwistrell i fesur cyfaint y nwy sy’n cael ei gynhyrchu.

Mae foltamedr Hofmann yn cael ei ddefnyddio’n aml i ddangos electrolysis meintiol dŵr. Serch hynny, mae’r rhain yn ddrud a does dim modd cyfiawnhau eu prynu i’w defnyddio bob hyn a hyn. Dewis arall yw creu fersiwn ar raddfa micro o chwistrelli plastig a thapiau 3-ffordd (ffigur 5).

Mae manylion sut mae gwneud y cyfarpar electrolysis ar raddfa micro a foltamedr Hofmann ar gael ar wefan CLEAPSS.
Mae manylion sut mae gwneud y cyfarpar electrolysis ar raddfa micro a foltamedr Hofmann ar gael ar wefan CLEAPSS.6
Rhagor o adnoddau
Learn Chemistry has a variety of electrolysis resources for students and teachers at all levels. Some provide further background information on industrial applications and include video clips filmed in industry.4 There are resources that show the historical development of electrolytic processes and theory.8 Other resources give details of experiments that have been tried and tested over many years.9 Also, Education in Chemistry has a demonstration to show the movement of ions.10
Mae gennym amrywiaeth o adnoddau electrolysis i fyfyrwyr ac i athrawon ar bob lefel, gan gynnwys…
- Gwybodaeth gefndirol am gymwysiadau diwydiannol, gyda chlipiau fideo wedi’u ffilmio mewn diwydiant.
- Ar y diwrnod hwn: Mae 4 Ionawr yn disgrifio datblygiad hanesyddol prosesau electrolytig.
- Arbrawf i adnabod cynhyrchion electrolysissydd wedi cael ei brofi yn yr ystafell ddosbarth.
- Tasg ymarferol i’r dosbarth i ymchwilio i symudiadau ïonau.
- Fideo ymarferol gyda chyfarwyddiadau integredig sy’n dangos electrolysis hydoddiannau dyfrllyd i ddysgwyr 14–16 oed.
- Cyngor ar osgoi camsyniadau cyffredin yn yr erthygl hon a’r ddalen waith gysylltiedig.
- Enghraifft o’r byd go iawn o ymchwil i electrolysis, gyda sleid crynhoi a chwestiynau i ddysgwyr 14–16 oed.
Mae David Everett yn athro cemeg sydd wedi ymddeol ac mae bellach yn gweithio fel ymgynghorydd addysg gwyddoniaeth annibynnol
References
- List of countries by aluminium production: bit.ly/2rxA8SW
- The essential chemical industry – chlorine: bit.ly/2rDjpbW
- The essential chemical industry – sodium hydroxide: bit.ly/2tu3vSo
- Alchemy? rsc.li/2tufMWS
- Electrolysing molten lead(II) bromide rsc.li/2sFr668
- CLEAPSS: science.cleapss.org.uk
- Redox: reducing difficulties eic.rsc.org/2000011.article
- On this day in chemistry: rsc.li/2rCCFGC
- Identifying the products of electrolysis: rsc.li/2shtLQv
- Migration of coloured ions: eic.rsc.org/2020064.article
- List of countries by aluminium production
- The essential chemical industry – chlorine
- The essential chemical industry – sodium hydroxide










No comments yet