Defnyddiwch y gwaith ymarferol lliwgar hwn i gyflwyno’r dysgwyr i electrolysis heli, neu hydoddiant sodiwm clorid
This resource is also available in English
Get the English language version.
Yn yr arbrawf hwn, bydd y dysgwyr yn arsylwi beth sy’n digwydd yn ystod electrolysis heli (hydoddiant sodiwm clorid), gan ddefnyddio dangosydd cyffredinol i’w helpu i ddilyn yr adwaith.
Mae’r arbrawf yn gweithio’n dda os ydych chi’n cyfarwyddo’r dysgwyr i wneud arsylwadau manwl ac yna i geisio egluro beth maent yn meddwl sy’n digwydd.
-

Lawrlwythwch
Lawrlwythwch y taflenni gwaith i fyfyrwyr (rhai wedi’u sgaffaldio a heb eu sgaffaldio), a’r canllawiau i athrawon (gan gynnwys yr atebion), ar ffurf MS Word a pdf a sleidiau’r cyflwyniad ar ffurf MS Powerpoint a pdf.
Darganfod rhagor o adnoddau o gasgliad gwaith ymarferol Nuffield
Amcanion dysgu
- Ymchwilio’n ddiogel i electrolysis heli.
- Nodi a disgrifio eich arsylwadau ar gyfer electrolysis heli.
- Defnyddio eich dealltwriaeth o electrolysis i egluro eich arsylwadau a’r cynhyrchion sy’n cael eu ffurfio.
- Rhagfynegi’r cynhyrchion fydd yn cael eu ffurfio.
Sgaffaldio
Ceir dau fersiwn o’r daflen waith i fyfyrwyr: fersiwn wedi’i sgaffaldio (✪) a fersiwn heb ei sgaffaldio (✪✪). Mae’r daflen wedi’i sgaffaldio yn cynnig mwy o gymorth i alluogi’r dysgwyr i ddeall y cwestiynau. Mae’r gwaith ymarferol yn creu llwyth gwybyddol mawr ac mae’n bosibl y bydd rhai dysgwyr yn cael trafferth cysylltu eu harsylwadau â’r theori.
Mae’r pwnc hwn yn gofyn am ddealltwriaeth dda o electrolysis ymlaen llaw, ac mae hynny’n gofyn am ddealltwriaeth dda o ïonau, cyfansoddion ïonig, priodweddau cyfansoddion ïonig a dangosyddion/pH.
Mae rhagfynegi’r cynhyrchion yn ystod electrolysis hydoddiannau dyfrllyd yn bwnc anodd, felly mae’r rheolau wedi’u cynnwys er mwyn helpu’r dysgwyr. Os oes angen, modelwch y rheolau hyn gydag ambell enghraifft cyn i’r dysgwyr wneud eu rhagfynegiadau.
Cyfarpar
Cyfarpar
- Sbectol diogelwch
- Tiwb profi siâp U
- Clamp a stand clamp
- Electrodau carbon a dalwyr electrod, x 2 (Os nad oes dalwyr electrod ar gael, gellid defnyddio dull addas arall o ddal yr electrodau yn eu lle. Peidiwch â defnyddio topynnau, gan mai nwyon yw’r cynhyrchion.)
- Lidiau trydanol, x 2
- Pecyn pŵer (foltedd isel, DC)
- Bicer, 100 cm3
- Sbatwla
- Rhoden droi
Cemegion
- Sodiwm clorid (halen cyffredin)
- Hydoddiant dangosydd cyffredinol (FFLAMADWY)
- Dŵr distyll (Os yw dŵr distyll yn broblem, gellid defnyddio dŵr tap. Ond gall effeithio ar y lliwiau fydd yn cael eu cynhyrchu, yn enwedig mewn ardaloedd dŵr caled.)
Nodiadau iechyd a diogelwch a nodiadau technegol
- Darllenwch ein canllawiau iechyd a diogelwch safonol a chynnal asesiad risg cyn gwneud unrhyw waith ymarferol byw.
- Gwisgwch sbectol diogelwch drwy gydol y gwaith, yn enwedig wrth glirio’r arbrawf. Mae cynhyrchion electrolysis yr hydoddiant halwyn i gyd yn fwy peryglus na’r deunyddiau cychwynnol.
- Mae hydrogen, H2 (n), yn EITHRIADOL O FFLAMADWY. Gweler Hazcard HC048 CLEAPSS neu dilynwch gyngor eich corff cynghori lleol ar ddiogelwch.
- Mae clorin, Cl2 (n), yn DOCSIG ac yn BERYGLUS I’R AMGYLCHEDD. Gweler Hazcard HC022a CLEAPSS neu dilynwch gyngor eich corff cynghori lleol ar ddiogelwch.
- Mae sodiwm hydrocsid, NaOH (dyfr ), yn GYRYDOL. Gweler Hazcard HC091a CLEAPSS neu dilynwch gyngor eich corff cynghori lleol ar ddiogelwch.
Gwnewch yn siŵr bod y cerrynt yn cael ei ddiffodd cyn gynted ag y bydd mymryn o glorin yn cael ei ganfod. Gall clorin fod yn broblem i ddisgyblion sy’n dioddef o asthma. Os dilynir y cyfarwyddiadau yn y weithdrefn, dim ond ychydig iawn o glorin fydd yn cael ei gynhyrchu.
Gweithdrefn
- Rhowch tua 75 cm3 o ddŵr distyll yn y bicer. Ychwanegwch ddau sbatwla gorlawn o sodiwm clorid.
- Trowch nes bod yr halwyn yn hydoddi . Yna ychwanegwch sawl diferyn o hydoddiant dangosydd cyffredinol. Trowch i’w gymysgu’n drylwyr. Bydd arnoch angen digon o ddangosydd i droi’r dŵr yn lliw gwyrdd eithaf cryf.
- Arllwyswch yr hydoddiant halwyn â lliw arno i mewn i’r tiwb profi siâp U a’i glampio fel y dangosir yn y diagram.
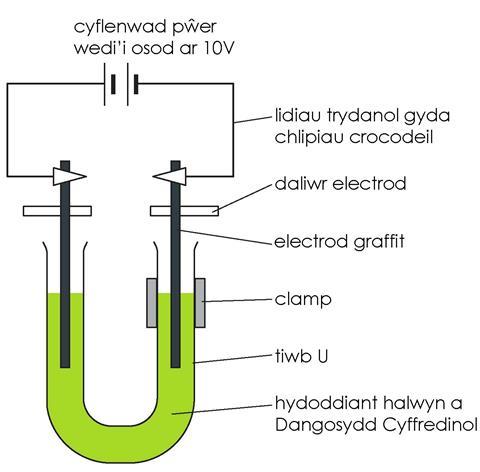
- Golchwch yr electrodau carbon yn ofalus mewn dŵr distyll ac yna’u gosod yn eu lle fel bod tua 3 cm o electrod ym mhob ochr o’r tiwb-U – gweler y diagram. Y ffordd hawsaf o wneud hyn yw drwy ddefnyddio dalwyr electrod.
- Cysylltwch lidiau â’r electrodau a’u cysylltu â phecyn pŵer sydd wedi’i osod ar 10 V (DC).
- Trowch y pecyn pŵer ymlaen ac arsylwi’n ofalus ar yr hyn sy’n digwydd. Gall fod yn ddefnyddiol dal darn o bapur gwyn y tu ôl i’r tiwb-U. Gwnewch yn siŵr bod y tiwb-U yn cael ei gadw’n hollol lonydd yn ystod yr arbrawf.
- Diffoddwch y pŵer cyn gynted ag y byddwch yn sylwi ar unrhyw newid wrth yr electrod positif, neu pan fyddwch yn arogli arogl ‘cannydd, tebyg i bwll nofio’. Bydd hyn yn cymryd llai na phum munud, fwy na thebyg.
Nodiadau i athrawon
Mae’r arbrawf hwn yn gyflwyniad diddorol i electrolysis heli. Peidiwch â’i ddefnyddio fel yr electrolysis cyntaf y bydd y dysgwyr yn ei weld. Byddai’n anodd iddynt egluro beth sy’n digwydd ar eu pen eu hunain. Gallwch astudio electrolysis hydoddiant halwyn mewn diwydiant ar ôl y gwaith ymarferol hwn.
Bydd swigod nwy i’w gweld wrth bob electrod. Wrth yr electrod positif, bydd y dangosydd yn troi’n goch i ddechrau ac yna’n cael ei gannu fel ei fod yn ddi-liw. Mae hyn yn dangos bod clorin yn bresennol. Wrth yr electrod negatif, bydd y dangosydd yn troi’n borffor. Bydd gweddill yr hydoddiant yn aros yn wyrdd.
Hydrogen yw’r cynnyrch wrth yr electrod negatif. Gall hyn fod yn anodd i’r dysgwyr ei ddeall.
Bydd rhywfaint o’r dŵr yn ïoneiddio, hynny yw, yn troi’n ïonau hydrogen (H+) a hydrocsid (OH–).
Pan fydd y sodiwm clorid yn cael ei hydoddi mewn dŵr, mae’r ïonau sy’n ffurfio’r solid ïonig yn gwahanu. Mae hyn yn golygu bod pedwar ïon yn bresennol yn yr hydoddiant: H+, OH–, Na+ a Cl–.
Mae’r ïonau negatif yn cael eu denu at yr electrod positif. Mae’r ïonau clorid yn cael blaenoriaeth o ran eu dadwefru (gan roi clorin) ar draul yr ïonau hydrocsid. Mae’r rhain yn cael eu gadael yn yr hydoddiant.
Wrth yr electrod negatif, mae’r ïonau hydrogen yn cael blaenoriaeth o ran eu dadwefru (gan gynhyrchu nwy hydrogen) ar draul yr ïonau sodiwm. Mae’r rhain hefyd yn cael eu gadael yn yr hydoddiant. Felly hydoddiant sodiwm hydrocsid sydd ar ôl. Dyma pam mae lliw porffor ar y dangosydd wrth yr electrod negatif.
Ymhen amser, byddai lliw gwyrdd y dangosydd yn y canol yn newid hefyd, wrth i’r ïonau dryledu drwy’r hydoddiant sydd wedi cael ei greu.
Hafaliadau
2H+ + 2e–→ H2 [electrod negatif, catod]
2Cl–→ Cl2 + 2e– [electrod positif, anod]
H2 O → H+ + OH–
Atebion
Mae’r atebion i’r cwestiynau yn y taflenni i fyfyrwyr ac ar sleidiau’r wers ar gael yn y nodiadau i athrawon.
Downloads
Electrolysis heli: taflen myfyriwr
Handout | PDF, Size 0.33 mbElectrolysis heli: taflen myfyriwr wedi ei sgaffaldio
Handout | PDF, Size 0.4 mbElectrolysis heli: nodiadau i athrawon
Handout | PDF, Size 0.45 mbElectrolysis heli: sleidiau gwers
Presentation | PDF, Size 0.73 mbElectrolysis heli: taflen myfyriwr
Editable handout | Word, Size 0.56 mbElectrolysis heli: taflen myfyriwr wedi ei sgaffaldio
Editable handout | Word, Size 0.55 mbElectrolysis heli: nodiadau i athrawon
Editable handout | Word, Size 0.57 mbElectrolysis heli: sleidiau gwers
Presentation | PowerPoint, Size 0.38 mb
References
Additional information
Daw’r adnodd hwn o’r prosiect Cemeg Ymarferol, sydd wedi cael ei ddatblygu gan Sefydliad Nuffield a’r Gymdeithas Gemeg Frenhinol. Mae’r casgliad hwn o dros 200 o weithgareddau ymarferol yn arddangos ystod eang o gysyniadau a phrosesau cemegol. Mae pob gweithgaredd yn cynnwys gwybodaeth gynhwysfawr i athrawon a thechnegwyr, gan gynnwys nodiadau technegol llawn a gweithdrefnau cam wrth gam. Mae’r gweithgareddau Cemeg Ymarferol yn cyd-fynd â’r rhai Practical Physics a Practical Biology.
Mae’r arbrawf hefyd yn rhan o gwrs Datblygiad Proffesiynol Parhaus y Gymdeithas Gemeg Frenhinol: Cemeg i rai nad ydynt yn arbenigwyr.
© Sefydliad Nuffield a’r Gymdeithas Gemeg Frenhinol
















No comments yet