O adeiladu sylfeini da i gofio’r rheolau, dyma ambell awgrym i helpu eich myfyrwyr i ddeall y pwnc anodd hwn
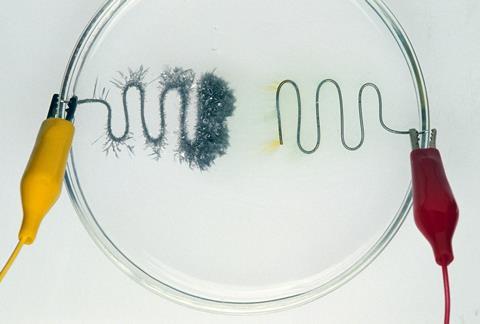
Mae etymoleg y gair electrolysis yn glir: electro sy’n golygu defnyddio trydan a lysis o’r Groeg sy’n golygu ‘hollti, llacio, rhyddhau’. Cafodd y term ei fathu gan Michael Faraday yn y bedwaredd ganrif ar bymtheg, ond roedd y broses ei hun yn cael ei defnyddio i astudio elfennau ymhell cyn hynny. Serch hynny, doedd ddim rhaid i’r gwyddonwyr hynny ateb cwestiynau arholiad ar y pwnc. Ac electrolysis yw un o’r pynciau anoddaf i fyfyrwyr 14-16 oed ei ddeall.
This article is also available in English
Read the English language version.
Pam ei fod mor anodd?
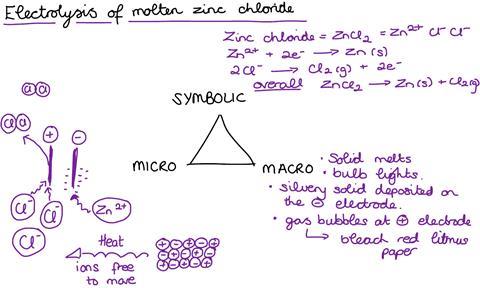
Mae electrolysis yn gysyniad haniaethol. Drwy arsylwi ar electrolysis yn y labordy, gall myfyrwyr weld tystiolaeth o’r cynhyrchion. Gallai hyn fod naill ai drwy arsylwi’n uniongyrchol ar fetel yn allddodi neu drwy ddefnyddio prawf, fel papur litmws, sy’n gallu dangos beth yw nwy di-liw. Serch hynny, mae angen iddyn nhw ddatblygu llun yn eu meddwl o’r hyn sy’n digwydd yn y cyfansoddion tawdd neu’r hydoddion. Mae’n enghraifft glasurol o bŵer triongl Johnstone wrth ddatblygu dealltwriaeth.
Mae’r llun hwn yn eu meddwl yn cynnwys cydrannau yn y parthau microsgopig a symbolaidd, gyda phob un yn dibynnu’n drwm ar wybodaeth flaenorol. Os oes unrhyw ran o’r wybodaeth flaenorol honno’n sigledig yna gall hynny danseilio eu dealltwriaeth o’r broses.
Dyma bum syniad i’ch helpu i’w gwneud hi’n haws i’ch myfyrwyr ddeall electrolysis.
1. Gwahanu cyfansoddion
Mae myfyrwyr iau yn dysgu nad oes modd gwahanu cyfansoddion i’w helfennau drwy ddulliau ffisegol (hidlo, anweddu ac ati) ac mae hon yn ffaith sy’n glynu. Felly mae’n gallu bod yn eithaf anodd deall bod electrolysis yn gallu gwahanu cyfansoddion i’w helfennau. I oresgyn y rhwystr meddyliol hwn, mae’n well cydnabod bod eu ffordd nhw o feddwl yn gywir ac yna egluro nad yw electrolysis yn ffitio’r diffiniad o ddull gwahanu ffisegol ac felly nid yw’r rheol honno’n berthnasol.
2. Gosod y sylfeini
Cyn i chi fynd i’r afael ag unrhyw gysyniadau newydd mewn electrolysis, gwnewch yn siŵr bod eich dosbarth yn deall sylfeini’r pwnc. Mae’n gallu teimlo bod mynd yn ôl at y pethau sylfaenol hyn yn eich arafu o ran symud ymlaen drwy’r cwricwlwm, ond byddwch yn ennill yr amser hwnnw’n ôl gyda chynnydd mwy effeithlon yn nes ymlaen.
Mae angen i’r myfyrwyr fod yn hyderus yn eu dealltwriaeth o natur gwefrau ïonig: pam mae ïon hydrogen yn bositif? Mae hyn yn eu helpu i gydbwyso hanner hafaliadau drwy ddefnyddio electronau yn nes ymlaen yn y pwnc. Dylen nhw hefyd fod yn gadarn gyda’r model bondio ïonig a sut mae priodweddau cyfansoddion ïonig yn ymwneud â hyn (yn enwedig o ran dargludo trydan).
Mae hefyd angen i’r myfyrwyr fod â gwybodaeth dda o’r gyfres adweithedd o fetelau; pa fetelau sy’n adweithiol iawn a pha rai sy’n llai adweithiol. Mae hyn yn bwysig wrth gyflwyno electrolysis hydoddion, er mwyn iddynt allu gweld ai hydrogen neu’r metel sy’n cael ei ryddhau wrth electroleiddio hydoddiant ac ystyried a yw’r electrodau yn anadweithiol.
Mae angen i’r myfyrwyr hefyd gael synnwyr o ffurf elfennau gwahanol; sut gallen nhw edrych pan fyddan nhw’n cael eu rhyddhau a pha rai sy’n foleciwlaidd.
3. Yn araf bach
Mae’n syniad da rhannu’r pwnc yn gydrannau ac addysgu pob darn yn fanwl, gan ailadrodd yr hyn a ddysgwyd yn flaenorol cyn ychwanegu’r haen nesaf o gymhlethdod. Mae arddangosiadau a gwaith ymarferol yn y dosbarth yn gallu helpu myfyrwyr i greu atgofion cryfach, gan gysylltu’r diriaethol â’r haniaethol. Mae hyn yn arbennig o ddefnyddiol wrth ddeall symudiadau ïonau ac mae modd delweddu hyn naill ai drwy ddefnyddio ïonau lliwgar iawn – edrychwch ar Tasg ymarferol mudiad ïonau i weld sut mae gwneud hyn – neu gyda dangosydd, fel y gwelir yn y Gweithgaredd electrolysis lliwgar hwn. Cynlluniwch wersi’n ofalus i sicrhau bod y gwaith ymarferol yn bwrpasol a bod amser i gysylltu’r canlyniadau â’r ddamcaniaeth.
Mae’n syniad da rhannu’r pwnc yn gydrannau ac addysgu pob darn yn fanwl, gan ailadrodd yr hyn a ddysgwyd yn flaenorol cyn ychwanegu’r haen nesaf o gymhlethdod. Mae arddangosiadau a gwaith ymarferol yn y dosbarth yn gallu helpu myfyrwyr i greu atgofion cryfach, gan gysylltu’r diriaethol â’r haniaethol. Mae hyn yn arbennig o ddefnyddiol wrth ddeall symudiadau ïonau ac mae modd delweddu hyn naill ai drwy ddefnyddio ïonau lliwgar iawn – edrychwch ar Tasg ymarferol mudiad ïonau (rsc.li/2Z2rgUj) i weld sut mae gwneud hyn – neu gyda dangosydd, fel y gwelir yn y Gweithgaredd electrolysis lliwgar hwn (rsc.li/3gsZDtt). Cynlluniwch wersi’n ofalus i sicrhau bod y gwaith ymarferol yn bwrpasol a bod amser i gysylltu’r canlyniadau â’r ddamcaniaeth.
Mae efelychiadau’n gallu helpu myfyrwyr i ddatblygu’r llun sydd ganddyn nhw yn eu meddwl yn y parth microsgopig, ar lefel gronynnau.
4. Ysgrifennwch hanner hafaliadau
Mae dau gam i’r broses o ysgrifennu hanner hafaliad:
- Cydbwyso’r atomau gan ddefnyddio cyfernodau yn ôl yr angen.
- Cydbwyso’r gwefrau drwy ychwanegu electronau at yr ochr gywir.
Mae hon yn broses syml i arbenigwr fel athro, ond mae sawl man lle gall dechreuwyr lithro. Yn aml bydd myfyrwyr yn dechrau drwy ychwanegu electronau. Mae llawer o’r nwyon a gynhyrchir mewn electrolysis yn ddeuatomig, ac mae’n hawdd i fyfyrwyr anghofio hyn, sy’n arwain at nifer anghywir o electronau yn yr hanner hafaliad.
5. Cofio’r rheolau
Mae rhai o’r rheolau, fel ïonau positif yn mynd i’r electrod negatif ac i’r gwrthwyneb, yn eithaf greddfol. Mae eraill, yn enwedig y rhai sy’n ymwneud â rhyddhau anionau, yn anoddach. Does dim byd gwell nag ymarfer yn fan hyn; modelwch eich ffordd o feddwl a’r cwestiynau byddwch chi’n gofyn i chi’ch hun pan fyddwch chi’n mynd i’r afael â chwestiwn electrolysis. Weithiau bydd methu cofio’n dal myfyrwyr yn ôl, felly rhowch drefnydd gwybodaeth i’r rhai sy’n cael trafferth cofio, yna wrth i’w hyder gynyddu gallwch dynnu’r sgaffaldau hyn i weld a ydyn nhw’n gallu cofio’r rheolau’n well.
Rhagor o adnoddau
- Dysgwch ragor am rôl Emma sy’n dechnegydd labordy biodrwytholchi ac yn casglu ac yn prosesu metelau gwerthfawr sy’n cael eu hechdynnu o gynhyrchion gwastraff electronig.
- Rhowch gynnig ar ddull gweithredu ar raddfa micro gyda thasg ymarferol sydd â chyfarwyddiadau integredig.
- Rhowch hwb i’ch DPP gyda chanllaw addysgu electrolysis i ddysgwyr 14–16 oed.
- Gwyliwch arddangosiad a dau arbrawf i ddysgwyr mewn fideo ar gyfres adweithedd metelau.













No comments yet